本维莫德是冷门的银屑病(俗称“牛皮癣”)治疗药。牛皮癣是一种免疫介导的慢性皮肤病,不易根治。
全球2~3%的人口深受这种疾病的折磨,有报道称,中国银屑病患者约800万人,实际数字可能更大。
.jpg)
VTAMA的生产由赛默飞和GSK提供
这款药,也是二十五年来,美国首次推出针对银屑病的外用新型化学药。
.jpg)
国内创新药研发的天花板
5月24日,美国FDA批准DermavantSciences公司的VTAMA®(tapinarof)乳膏用于治疗成人斑块状银屑病。
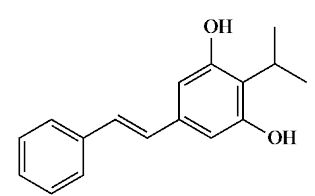
本维莫德结构式(海外名称:tapinarof)
本维莫德(商品名:欣比克,曾用名:苯烯莫德)是一种芳香烃受体调节剂,最早是在中国诞生(获批上市),上市许可持有人为冠昊生物科技股份有限公司(股票代码300238)旗下的控股子公司广东中昊药业有限公司。
2012年,葛兰素史克花费2.3亿美元购得本维莫德除中国大陆、台湾、香港和澳门市场以外的市场开发权。
2018年7月,葛兰素史克以3.3亿美元的价格向Dermavant出售了这一权益。
2019年5月,本维莫德乳膏在中国首先上市,用于局部治疗成人轻至中度稳定性寻常型银屑病。
本维莫德乳膏是中国近十年批准上市的三款First In Class的创新药之一,也是目前为止,在中国率先批准上市之后才获美国FDA批准的首款创新药。
时代浪潮的洗礼
上世纪90年代,加拿大西蒙弗雷泽大学共生菌研究实验室中,陈庚辉团队从一种土壤线虫的共生细菌代谢产物中分离出来了一种小分子化合物,对银屑病治疗有积极作用。

左:John M. Webster 中:陈庚辉 右:李健雄(图片来源:SFU.CA)
一开始,团队致力于将该化合物做成体内用药。但随后他们发现,进入人体后,这个化合物很快就会被代谢出去,更无从谈治疗效果。
一般这时候,有两种思路:
一是重新改进化学结构;
二是做成复杂的制剂,让药物缓释。
但非医药学的出身的陈庚辉决定将该化合物制成体外用药。本维莫德的化合物分子很小,容易被皮肤吸收,并且它还具有与人的角质层相同的脂溶性。
作为一个生物学家,陈庚辉另辟蹊径的解决思路,是本维莫德诞生的第一步。
2009年,陈庚辉辞掉了Welichem Biotech公司CEO的职位选择回国,开始推进本维莫德的临床研究。
2010年前后,正是国内创新药研发如火如荼的时刻,只要有技术,就一只脚迈进了成功的大门。
但陈庚辉并非如此,他看准了北大人民医院皮肤科主任张建中大夫,希望其牵头做临床研究。
然而,没有实验室,没有临床研究的经验,彼时的他只能在医院里一次次等待,换来与张大夫短暂沟通交流的机会。
从一开始表现得“像个骗子”,再到后来被张建中大夫认可推进临床研究,陈庚辉骨子里的血性和坚韧,奠定了研发成功的基础。
总结
21年9月,陈庚辉博士从广东中昊药业离职了。
广东中昊药业是冠昊生物旗下子公司,拥有本维莫德在中国市场的权益,冠昊生物2021年年报显示,本维莫德去年销量近40万支,营收2992.74万元。
随着该药在美国获批上市,本维莫德的商业价值也将进一步被证明。
本维莫德作为全球首创、拥有完整自主知识产权的1类新药,为成人轻至中度稳定性寻常型银屑病患者提供一种新的药物治疗手段,有望发展成为市场规模达10亿元以上的大品种。
回望过去,1995年拿到第一个专利证书,陈庚辉实现了科学家的发明梦;研发二十年在国内收获了国家1类新药证书,他实现了新药研发者的中国梦。
坐得住冷板凳,也能从容接受鲜花与掌声。到目前为止,我国先批准上市而后美国FDA才批准的创新药,陈庚辉是第一人。
2021年8月10日,Dermavant Sciences公司宣布,FDA受理创新药Tapinarof(本维莫德在海外的名称)上市申请(NDA),用于治疗银屑病成人患者,PDUFA(处方药付费法案)日期为2022年第二季度。
欧洲,日本和其它国家也将相继上市,届时本维莫德将成为真正意义的全球创新药,在皮肤科外用药领域具有划时代意义。